Высокая технология производства филлеров
состоит из большого количества процессов и этапов.
Есть технологии, которые позволяют изготавливать филлеры за 48 часов. Это, конечно, дает преимущество в стоимости продукта. Но мы не позволяем себе спешить. Мы считаем, что планомерное и полноценное прохождение всех этапов очень важно. И ни один из них нельзя сократить, не рискуя при этом качеством препаратов.
К примеру, мы не можем сократить этап очистки или этапы связанные со сшивкой гиалуроновой кислоты (ГК). Если после сшивки ГК плохо очищена от вещества, которым сшивается, филлер будет иметь высокий остаточный BDDE и может дать осложнения.
Мы изготавливаем филлеры 21 день: 14 дней занимает сам производственный процесс и 7 дней — проверки.
Такой подход позволяет нам выпускать препараты с точно выверенными характеристиками и избавить врачей и пациентов от рисков.
HTL Biotehnology на рынке уже 25 лет. Компания сертифицирована GMP (good manufacturing practice, требования к производству лекарственных средств и медицинских изделий) и контролирует качество своего продукта по фармакопее: чистая гиалуроновая кислота, получаемая ферментацией из естественных непатогенных стрептококков, без белков и эндотоксинов, не ГМО-штамм.
Гиалуроновая кислота безопасна, не вызывает аллергии и раздражения. Используется в офтальмологии, дерматологии и ортопедии.
Соответствует требованиям качества ЕС (европейская сертификация качества), регулирующих органов США, Австралии, Японии и других стран. В том числе требованиям Министерства здравоохранения России (ФС 000226-011111). Подробная информация о характеристиках продукта и самой компании доступна на официальном сайте производителя.
В дополнение мы проверяем каждую поступающую партию сырья на соответствие заявленным в спецификации характеристикам.

Например, остаточный BDDE (вещество, которым сшивают гиалуроновую кислоту в филлере для ее стабилизации).
В процессе сшивки часть его вступает в соединение с молекулами гиалуроновой кислоты, а часть — нет. Прореагировавший BDDE, полностью безопасен. Непрореагировавший, если он содержится в большом количестве, в некоторых случаях может вызывать побочные реакции и осложнения. Поэтому после сшивки остаточный BDDE вымывают с помощью комплекса очистительных процессов (у каждого производителя он свой).
В европейской фармакологии допустимым считается
содержание остаточного BDDE до 2 ppm.
Хорошим стандартом считается содержание BDDE не более 0.5 ppm.
Среднее оборудование в сочетании с методом исследования имеет предел обнаружения 0.5 — 0.8 ppm. «Не увидев» значения меньше 0,5 ppm, такая аппаратура может констатировать, что BDDE нет вообще. Но действительности это соответствовать не будет.
Мы используем газовый хромотограф с масс-детектером Agilent-GSMS, который имеет предел обнаружения — 0.25 ppm.
Это значительно строже допустимых стандартов.
Но позволяет нам гарантировать высокую чистоту и безопасность филлеров.
Каждый аппарат на производстве с периодичностью проверяется и калибруется производителем, результаты проверок записываются в контрольный журнал.


Ни один производственный этап не проводится в одиночку. Всегда задействованы как минимум два сотрудника: выполняющий и проверяющий.
Все данные записываются и анализируются при переходе с этапа на этап до мельчайших деталей.
И тем не менее, готовый продукт все равно проходит 11 проверок.
ISO 9001
Определяет требования для всех подразделений компании. Обязывает заниматься изучением отклонений от норм и выработкой корректирующих действий для предотвращения их в будущем.
Ставит целью постоянное совершенствование системы: разработку путей решения и мониторинг результатов по прошествии времени.
ISO 13485
Устанавливает высокие требования к безопасности выпускаемых изделий и валидированию всех производственных процессов.
Обязывает вести производственную документацию (какое сырье было использовано при производстве, из каких компонентов состоит продукт), что позволяет отследить историю всех выпущенных препаратов.
Отдельное подразделение производства —
департамент обеспечения качества.
Он независимый, то есть иерархически не подчинен руководству компании. Руководитель департамента ориентируется исключительно на регуляторные требования Европейского Союза и других стран.
Он может остановить любой процесс, отозвать любую партию филлеров. Даже из-за опечатки в одну букву на упаковке, если посчитает, что она несет неправильную информацию.
Мы проверяем и документируем каждый производственный процесс: от качества закупаемого сырья до условий транспортировки готового продукта.
Например, в производственных помещениях DKL 5-ый класс стерильности (ISO). Тем не менее мы производим бак-посев для каждого выпускаемого лота препаратов. Если в образце обнаружится хоть какая-либо микрофлора, вся партия будет уничтожена.
В целом каждый выпускаемый лот продукции проходит 11 аналитических и микробиологических проверок.
Для этого у нас есть собственные лаборатории: аналитическая (фокусируется на физических характеристиках препаратов: таких как вязкость, концентрация, PH, остаточный BDDE) и микробиологическая (обеспечивает безопасность наших продуктов: важно чтобы препарат был стерилен, чист от эндотоксинов).
Собственные лаборатории есть не у всех компаний, так как их сложно и дорого обслуживать.
Но сторонние лаборатории не находятся в тесном взаимодействии с производством и не знают досконально все нюансы продукта. А значит не всегда могут достоверно его проверить. Кроме того проверки проводятся по собственным параметрам сторонних лабораторий, и заключения могут оказаться искаженными даже при наличии большого количества инструкций.
Собственные лаборатории специализируются на конкретном продукте, существуют в одной системе координат с производством и могут однозначно протестировать соответствие. Качество препарата будет точно соответствовать заявленному.
Упаковка наших препаратов — медицинская пленка Tyvek 5G (600 микрон) немецкого производства. Она надежно защищает продукт и сохраняет стерильность шприца. Но для сохранения свойств самого филлера важна температура его транспортировки и хранения.
Логистические компании на каждом этапе перевозки и дистрибьюторы в каждой стране прошли валидацию и предоставляют соответствующую сопровождающую документацию по каждой партии.
Внутренние стандарты DKL по допустимым значениям параметров строже официальных допустимых значений. Если образец не прошел контроль — уничтожается вся партия.
Это гарантия для врачей и клиентов, что они не встретят продукт низкого качества.
Это касается не только R&D и ключевых вопросов.
Нам важно видеть изнутри, как идет каждый процесс.
Например, медицинский директор может встать на линию упаковки и пройти весь рабочий цикл этого этапа, а маркетинговый директор участвует в разборе обратной связи от региональных дилеров в каждой стране.
На производстве настроена круглосуточная система оповещения. Датчики установлены в каждом помещении и на ключевом оборудовании. Если какой-либо из параметров приближается к пограничному значению, сразу нескольким ответственным сотрудникам приходят сообщения.
Мы ежегодно проводим анкетирование врачей. Собираем обратную связь о непосредственной работе с препаратами и комплектующими, о результатах, которых удалось достичь, истории, отзывы и пожелания клиентов.
Эта обратная связь служит для нас не менее важным основанием, чем научные разработки.
Будем рады вашим отзывам и вопросам!

основатель и генеральный директор Dr. Korman Laboratories

основатель и медицинский директор Dr. Korman Laboratories
Строгие внутренние проверки — часть общего контроля качества. Мы регулярно принимаем на производстве сторонние независимые проверки, аттестации и комиссии из регулирующих организаций стран, с которыми работаем.
В том числе сертификат MDSAP ISO 13485:2016.
Выдан компанией BSI и подтверждает соответствие системы качества компании Dr. Korman Laboratories регуляторным требованиям Канады, Австралии, Японии и других стран к разработке и производству медицинских изделий.
В 2013 году филлеры Dr.Korman Laboratories были сертифицированы в соответствие с директивой 93/42/ЕЕС, что гарантирует безопасность для здоровья человека.
С 2018 года мы проводим дополнительные клинические испытания наших препаратов в независимом холдинге CTC Clinical Trial Consultants AB (Швеция)
В России препараты прошли необходимые проверки, официально зарегистрированы и разрешены к применению Росздравнадзором.
и безопасность
Качество и характеристики препарата не меняются от партии к партии.
Врач может быть уверен в том, что содержимое шприца соответствует заявленным на упаковке значениям. А значит и в предсказуемости результата, который получит в каждом конкретном случае.
и прозрачность
Образец геля из каждой партии хранится в течение 5 лет вместе с документацией по его производству.
В случае какой-либо нестандартной ситуации мы готовы предоставить COA (сертификат анализа данного лота) или провести сравнительные анализы.
и назовите номер лота, указанный на шприце.
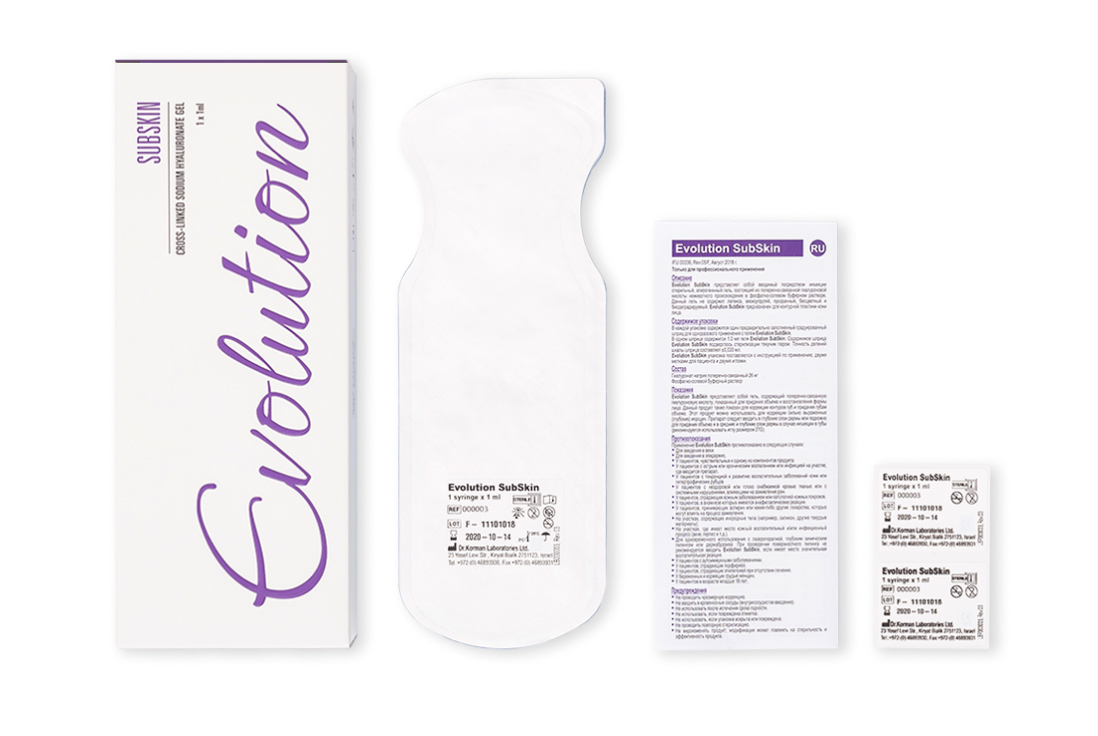
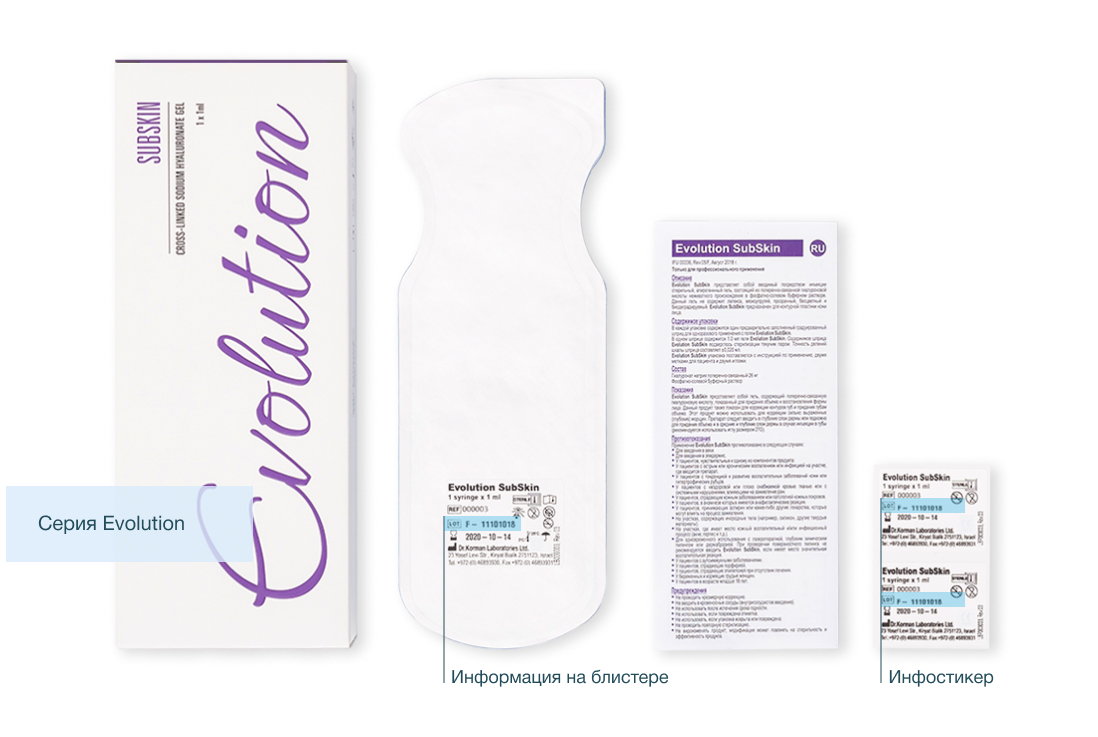
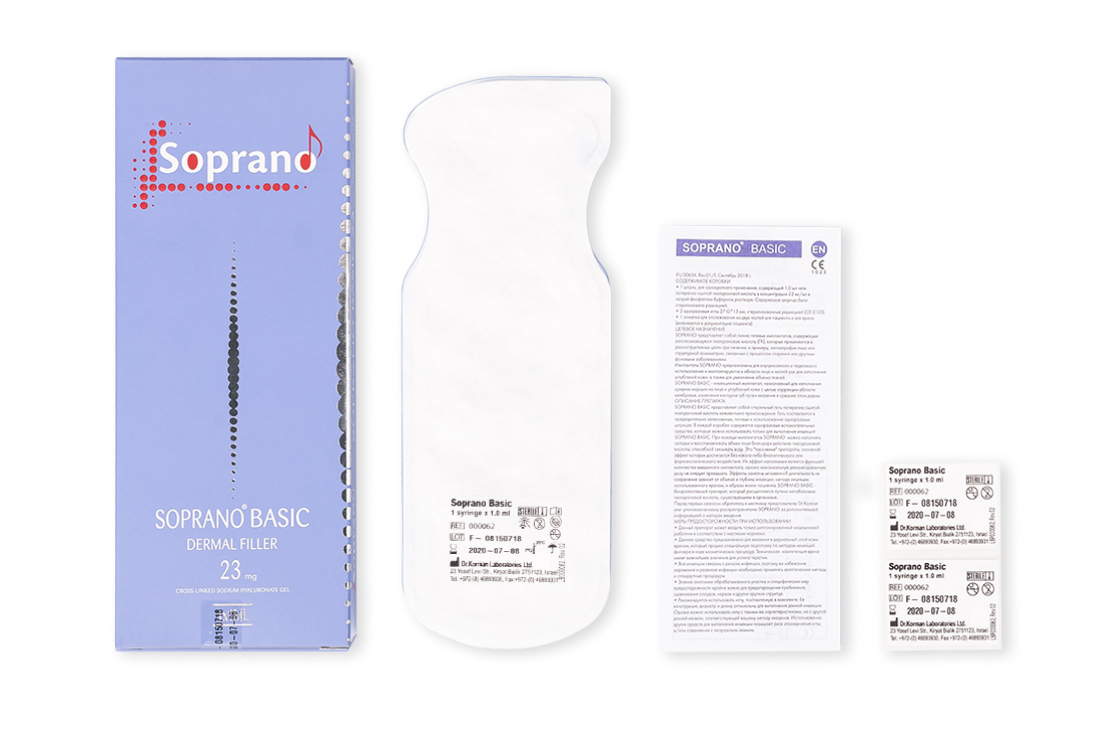
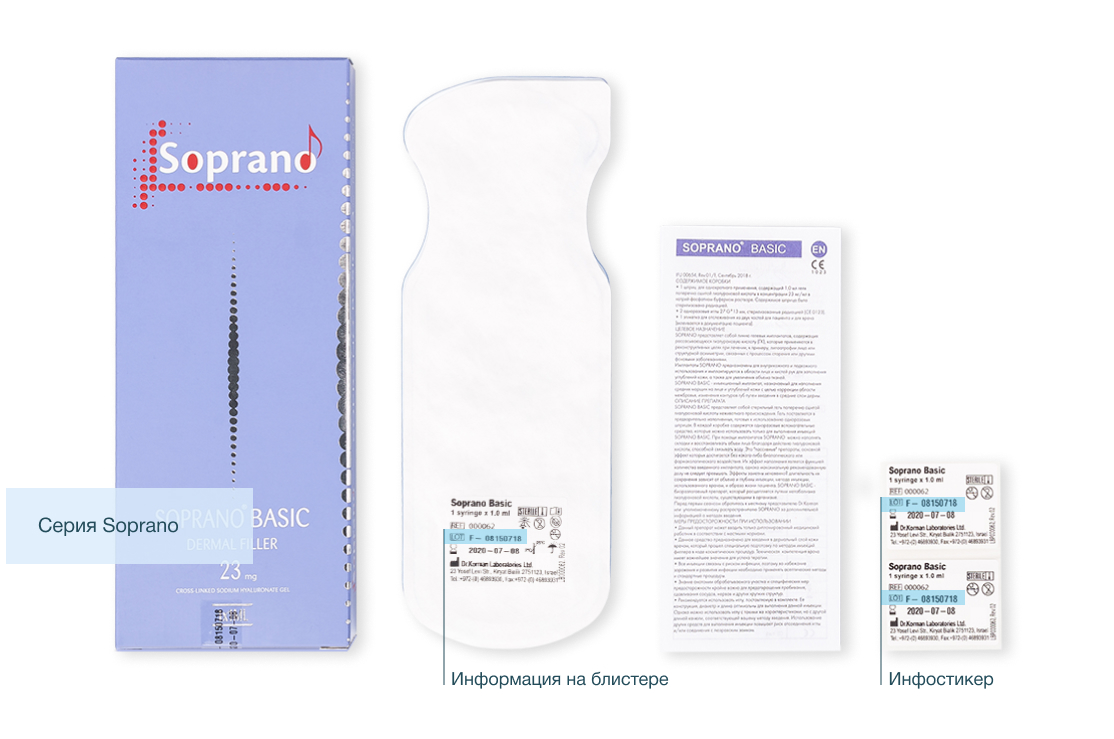
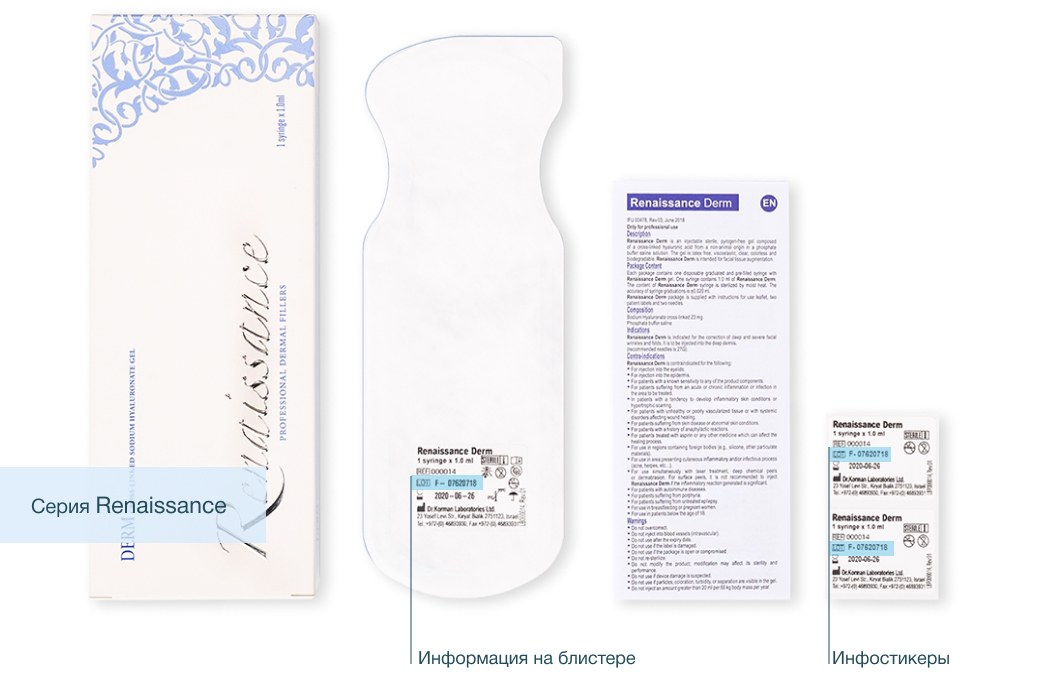
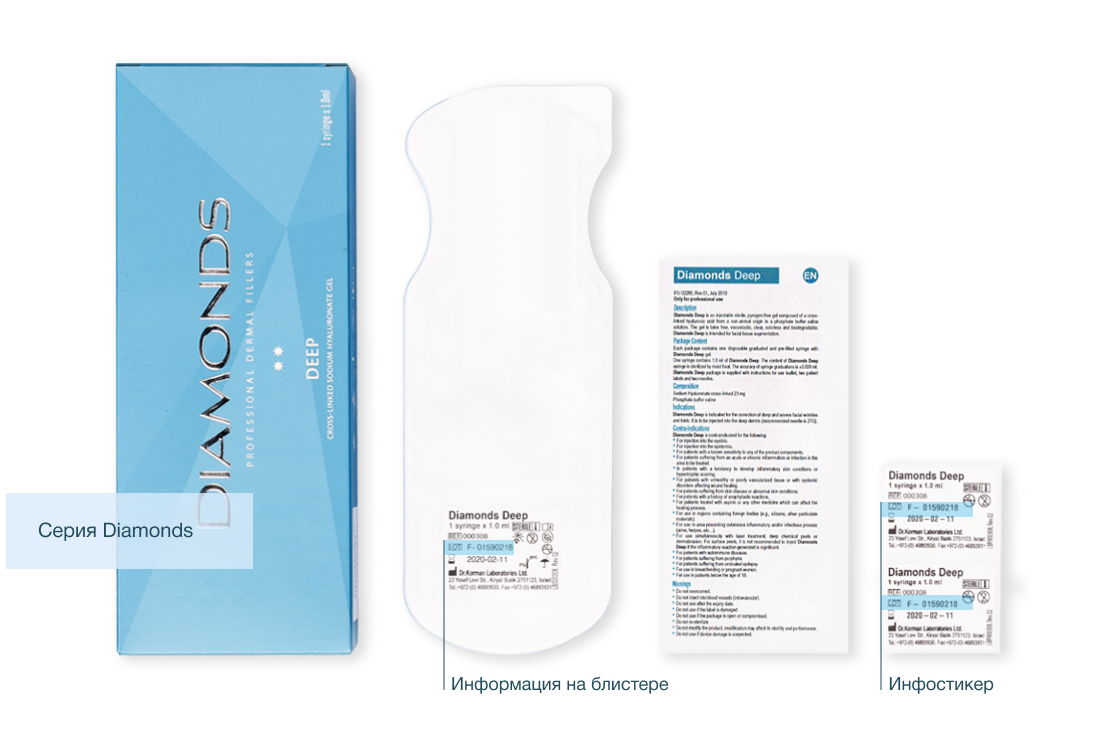
Как определить номер лота
Помимо шприца информация с номером лота указана на блистере.
Также в комплекте предоставляются 2 дополнительных инфостикера:
- для врача, чтобы можно было использовать ее в истории пациента,
- для самого пациента.
Нажав кнопку «Я врач», вы подтверждаете, что учли указания по использованию сайта и намерены ознакомиться с информацией, предназначенной только для врачей.